Faith Evans feat. Stevie J – "A Minute" [Official Music Video]
สารบัญ:
- วิธีการทำงานคือเซ็นเซอร์ CGM อ่านข้อมูลระดับน้ำตาลทุกห้านาทีและอัลกอริธึมลูปปิดที่ติดตั้งอยู่ในปั๊มจะใช้ข้อมูลดังกล่าวเพื่อเพิ่มหรือลดอินซูลินพื้นฐานเพื่อให้ระดับกลูโคสใกล้เคียงกับเป้าหมายที่ 120 mg / dL ผู้ใช้ยังคงต้องใส่ carb counts และ bolus ในมื้ออาหารและแจ้งเตือนล่วงหน้าก่อนการออกกำลังกายใด ๆ นอกจากนี้ยังไม่ได้ให้ boluses การแก้ไขโดยอัตโนมัติตาม CGM แต่จะแนะนำให้แก้ไขจำนวนเงินเมื่อผล fingerstick เป็น ป้อนเช่นเดียวกับเครื่องปั๊มอินซูลินมาตรฐานทั้งหมดในขณะนี้ผ่านคุณลักษณะ Bolus Wizard
- ตามที่ระบุไว้ลักษณะเป็นเหมือนกับ Minimed 630G ที่เพิ่งเปิดตัวเมื่อเดือนที่แล้ว (ล้าสมัยไปแล้ว) แบตเตอรี่ AA ชุดเดียวกันและชุดอินซูลิน 300 ชุดและมีขนาดเล็กกว่าเครื่องสูบแบบ Minimed แบบดั้งเดิมที่มีขนาดเล็กกว่าเล็กน้อยโดยมีแนวนอนอยู่ ในทางตรงกันข้ามกับเครื่องปั๊ม Medtronic รุ่นเก่าอุปกรณ์นี้จะนำเสนอเป็นสีดำเท่านั้น แต่คุณสามารถซื้อสกินหลายแบบเพื่อให้ได้ภาพลักษณ์ที่แจ๊สได้ตามต้องการ
- รวมค่าใช้จ่ายโปรแกรมกระเป๋า = เพียง $ 299
- Disclaimer
ว้าวสิ่งที่เป็นช่วงเวลาที่ยิ่งใหญ่สำหรับชุมชนโรคเบาหวาน!
เมื่อวันพุธ FDA ได้อนุมัติ Minimed 670G ของ Medtronic ซึ่งเป็นระบบไฮบริดลูปปิดที่มีการตรวจสอบระดับน้ำตาลในเลือดและปรับระดับอินซูลินในคนอายุตั้งแต่ 14 ปีขึ้นไปที่เป็นเบาหวานชนิดที่ 1

"นี่เป็นเรื่องมหัศจรรย์และฉันก็มีความสุขมาก! "Aaron Kowalski, Chief Mission Officer ของ JDRF และ longtime type 1 กล่าวว่า "มันน่าทึ่งมากที่ได้อยู่ในระดับนี้ (ระบบอัตโนมัติ) ได้รับการอนุมัติ … และระยะเวลาอันสั้นที่องค์การอาหารและยาต้องล้างข้อมูลนี้ "
อะไรคือระบบการควบคุมกลูโคสใหม่นี้และทำงานได้อย่างไร?
Loop Closed Loop คืออะไร?คำว่า "hybrid" ในกรณีนี้หมายถึงระบบนี้ทำงานโดยอัตโนมัติบางส่วน แต่ยังต้องมีการควบคุมโดยผู้ใช้
วิธีการทำงานคือเซ็นเซอร์ CGM อ่านข้อมูลระดับน้ำตาลทุกห้านาทีและอัลกอริธึมลูปปิดที่ติดตั้งอยู่ในปั๊มจะใช้ข้อมูลดังกล่าวเพื่อเพิ่มหรือลดอินซูลินพื้นฐานเพื่อให้ระดับกลูโคสใกล้เคียงกับเป้าหมายที่ 120 mg / dL ผู้ใช้ยังคงต้องใส่ carb counts และ bolus ในมื้ออาหารและแจ้งเตือนล่วงหน้าก่อนการออกกำลังกายใด ๆ นอกจากนี้ยังไม่ได้ให้ boluses การแก้ไขโดยอัตโนมัติตาม CGM แต่จะแนะนำให้แก้ไขจำนวนเงินเมื่อผล fingerstick เป็น ป้อนเช่นเดียวกับเครื่องปั๊มอินซูลินมาตรฐานทั้งหมดในขณะนี้ผ่านคุณลักษณะ Bolus Wizard
< ! - 1 ->
หน้า FDA นี้อธิบายรายละเอียดได้ดี ระบบ MiniMed 670G มีสองโหมดคือ "Autopilot" มากกว่าระบบอื่น ๆ แต่ทั้งคู่ต้องมีการแทรกแซงของผู้ใช้ (จึงไม่ใช่ลูปปิดอย่างสมบูรณ์):
Manual Mode- ระบบสามารถตั้งโปรแกรมโดย ผู้ใช้เพื่อส่งอินซูลินพื้นฐานที่อัตราคงที่ล่วงหน้าโปรแกรมระบบจะระงับการส่งอินซูลินโดยอัตโนมัติหากค่ากลูโคสของเซ็นเซอร์อยู่ต่ำกว่าหรือคาดว่าจะลดลงต่ำกว่าเกณฑ์ที่กำหนดไว้ ระบบจะดำเนินการจัดส่งอินซูลินโดยอัตโนมัติเมื่อค่ากลูโคสของตัวรับรู้สูงขึ้นหรือคาดว่าจะสูงกว่าเกณฑ์ที่กำหนดไว้
ผู้ใช้จะต้องจัดส่งอินซูลินในระหว่างมื้ออาหารด้วยตนเอง Minimed 670G มีลักษณะและเกือบจะเหมือนกันกับ Minimed 630G ที่ได้รับอนุมัติเมื่อเร็ว ๆ นี้ซึ่งนำแนวตั้งและหน้าจอสีใหม่มาสู่การออกแบบปั๊มมาตรฐานของ Medtronic ข้อมูลจำเพาะของผลิตภัณฑ์มีดังต่อไปนี้: หน่วยสูบ: ปุ่มและเมนู: ความแตกต่างเพียงเล็กน้อยระหว่าง 630G กับ MiniMed 670G ใหม่คือความจริงที่ว่าปุ่มบนขวาจะนำคุณไปยังกราฟ CGM โดยตรงกับเส้นทางไปยัง Menus และเมนูจะแตกต่างกันเล็กน้อย , ให้เลือกโหมดใหม่ ฯลฯ ในระบบใหม่ การมีส่วนร่วมในการสำรวจและโปรแกรมแสดงความคิดเห็นของผู้ใช้อื่น ๆ สามารถทำได้ ลดค่าใช้จ่ายที่ต่ำถึง $ 0 สำหรับบางคน บริษัท ฯ โปรแกรมการเข้าถึงความสำคัญเริ่มทำงานผ่าน 28 เมษายน 2017 Medtronic ยังกล่าวข้อเสนอเพิ่มเติมและความเป็นไปได้การปรับรุ่นอาจมีการเปิดเผยใกล้ชิดกับเวลาเปิดตัวในฤดูใบไม้ผลิ แน่นอน Medtronic จะทำงานในหลายเดือนข้างหน้ากับผู้จ่ายเงินและ บริษัท ประกันภัยในการให้ความคุ้มครองสำหรับเทคโนโลยีนี้ เมื่อมีข้อพิพาทเกี่ยวกับปัญหาเหล่านี้ (#DiabetesAccessMatters) เราหวังว่า Medtronic จะทราบว่าขณะที่ผู้ป่วยจำนวนมากต้องการระบบนี้ แต่ก็อาจไม่ใช่ทางเลือกที่ดีที่สุดสำหรับเรื่องทั้งหมดและเรื่องที่เลือก!
ในความเป็นจริง FDA ได้อนุมัติตลาดสำหรับ Minimag 670G นี้ในขณะที่ยังต้องการการศึกษาเพิ่มเติมในตลาดหลังการขายเพื่อให้เข้าใจถึงวิธีการทำงานของอุปกรณ์ในการตั้งค่าจริง ที่แสดงให้เห็น FDA ยินดีที่จะดูข้อมูลที่มีอยู่และไว้วางใจผลประโยชน์โดยไม่ต้องถือครองกลับสำหรับรีมของข้อมูลในอนาคต นอกจากนี้เรายังได้พูดคุยกับเจฟฟรีย์บรูเออร์ผู้ซึ่งดูแล Bigfoot Biomedical ซึ่งกำลังพัฒนาระบบลูปปิดที่คาดว่าจะสามารถใช้ได้ในช่วงปี 2018 พร้อมกับ Aaron Kowalski Brewer ถือเป็นหนึ่งใน "พ่อของ AP" ให้บทบาทของพวกเขาในการช่วยในการพัฒนาและส่งเสริมเส้นทางวงปิดที่ JDRF ไม่ต้องสงสัยเลยว่านี่จะทำให้เข็มไปข้างหน้ากับระบบลูปปิดอื่น ๆ อีกกว่า 18 แบบโดยเฉพาะอย่างยิ่งที่ใช้อินซูลินเท่านั้น บางคนจะเพิ่มฮอร์โมนกลูคากันเพิ่มเติมในการผสมเพื่อลดระดับน้ำตาลในเลือด (เช่น Beta Bionics iLET และ Pancreum Genesis) ซึ่งอาจจำเป็นต้องใช้เวลาในการประเมินผลของ FDA มากขึ้นตามที่ระบุไว้ลักษณะเป็นเหมือนกับ Minimed 630G ที่เพิ่งเปิดตัวเมื่อเดือนที่แล้ว (ล้าสมัยไปแล้ว) แบตเตอรี่ AA ชุดเดียวกันและชุดอินซูลิน 300 ชุดและมีขนาดเล็กกว่าเครื่องสูบแบบ Minimed แบบดั้งเดิมที่มีขนาดเล็กกว่าเล็กน้อยโดยมีแนวนอนอยู่ ในทางตรงกันข้ามกับเครื่องปั๊ม Medtronic รุ่นเก่าอุปกรณ์นี้จะนำเสนอเป็นสีดำเท่านั้น แต่คุณสามารถซื้อสกินหลายแบบเพื่อให้ได้ภาพลักษณ์ที่แจ๊สได้ตามต้องการ



ระบบได้รับการตั้งค่าเพื่อสื่อสารกับ Bayer Contour Link 2. 4 เมตรที่ Ascensia เปิดตัวพร้อมกับประกาศเปิดตัว 630G นี้จะช่วยให้การ bolusing ระยะไกลจากมิเตอร์ แต่เฉพาะในโหมด Manual มากกว่าใน Auto Mode แบบปิด
รวมค่าใช้จ่ายโปรแกรมกระเป๋า = เพียง $ 299
เป็นเรื่องที่ยอดเยี่ยมที่องค์การอาหารและยาได้ดำเนินการอย่างรวดเร็วไม่ใช่เฉพาะในการอนุมัติ Minimed 670G แต่ด้วยเทคโนโลยีด้านข้อมูลเบาหวานที่น่าตื่นเต้นอื่น ๆ และการพัฒนาข้อมูลในช่วงหลายปีที่ผ่านมา เห็นได้ชัดว่า FDA ตระหนักถึงการเคลื่อนไหวของ #WeAnNotWaiting และพยายามอย่างดีที่สุดเพื่อให้ทันกับเวลาที่เคลื่อนที่เร็วเหล่านี้

องค์การอาหารและยาอนุมัติ Libre Pro
เป็นที่น่าสังเกตว่า FDA ได้ให้แสงสีเขียวแก่ระบบ Abbott Freestyle Libre Pro ในสหรัฐฯเป็นระยะ ๆนี่ไม่ใช่อุปกรณ์สำหรับผู้บริโภค แต่เป็นเวอร์ชั่นแพทย์ของ Abbott เทคโนโลยีการตรวจสอบกลูโคสแบบแฟลช (FGM) ใหม่ซึ่งพร้อมให้บริการแก่ผู้ป่วยในต่างประเทศแล้ว
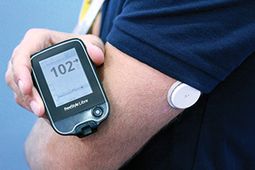
นอกจากนี้ยังเรียกว่าระบบ "ไฮบริด" - แต่สำหรับการตรวจสอบกลูโคสเท่านั้น - Abbott Libre ประกอบด้วยเซ็นเซอร์กลมขนาดเล็กที่สวมใส่ได้นานถึง 14 วันที่ด้านหลังของต้นแขนและตัวควบคุมที่ผู้ใช้เพียงแค่กวาดนิ้ว มากกว่านั้นเป็นหลาย ๆ ครั้งต่อวันตามที่ต้องการหรือต้องการที่จะอ่านแบบไร้สายกลูโคส
ไม่มีการแจ้งเตือนใด ๆ เกี่ยวกับการเพิ่มขึ้นหรือลดระดับน้ำตาลในเลือดและเวอร์ชันสำหรับผู้บริโภคในต่างประเทศจะจัดเก็บข้อมูลเพียง 8 ชั่วโมงจุดมุ่งหมายคือการสร้างโซลูชันการตรวจสอบที่เรียบง่ายขึ้นซึ่งจะช่วยให้หลายประเภท 2 สามารถติดต่อกับระดับน้ำตาลในแบบเรียลไทม์ได้มากขึ้นในขณะที่ไม่ใช่แนวคิดแบบดั้งเดิมของ CGM ตามที่เราทราบ Abbott กล่าวว่ากฏกติกาต่างๆระบุว่า Libre เป็น CGM และสิ่งที่พวกเขาได้อนุมัติตอนนี้ก็คือรุ่นที่ออกแบบมาเฉพาะสำหรับแพทย์ที่จะให้ยืมแก่ผู้ป่วยของพวกเขาสำหรับการใช้งานในระยะสั้นและจะให้ข้อมูลที่มองไม่เห็นสำหรับแพทย์เท่านั้น นี่เป็นก้าวแรกของรุ่นผู้บริโภคซึ่งแอ๊บบอตได้ยื่นขออนุมัติจาก FDA เมื่อเร็ว ๆ นี้ในสหรัฐฯ
หวังเป็นอย่างยิ่งว่าจะเร็ว ๆ นี้ด้วยการคิดค้นนวัตกรรมใหม่ ๆ ที่เพิ่มขึ้นอย่างรวดเร็วของ FDA
ขอขอบคุณทุกคนที่เกี่ยวข้องไม่น้อยกว่าที่ FDA สำหรับการย้ายเครื่องมือการดูแลผู้ป่วยโรคเบาหวานที่สำคัญเหล่านี้ไปข้างหน้าด้วยผลประโยชน์สูงสุดของเรา!คำปฏิเสธ
: เนื้อหาที่ทีม Diabetes Mine สร้างขึ้น สำหรับรายละเอียดเพิ่มเติมคลิกที่นี่
Disclaimer
โรคเบาหวาน Update: อุปกรณ์ Medtronic รุ่นใหม่ FDA อนุมัติ FDA

FDA อนุมัติอุปกรณ์ Medtronic ใหม่สำหรับผู้ป่วยเบาหวานที่สามารถปิดการจัดส่งอินซูลินได้โดยอัตโนมัติหาก น้ำตาลในเลือดต่ำเกินไป
NewsFlash: FDA อนุมัติ Animas Vibe

ดูสาเหตุที่ DiabetesMine รู้สึกตื่นเต้นมากเกี่ยวกับ Animas Vibe ซึ่งเป็นอุปกรณ์คำสั่งผสมที่รอคอยมานานที่รวม Dexcom G4 Platinum CGM และปั๊ม Animas Ping
FDA อนุมัติ iBGStar Meter สำหรับ iPhone / iPod Touch!



